Коррозия – разрушение поверхности сталей и сплавов под воздействием различных физико-химических факторов – наносит огромный ущерб деталям и металлоконструкциям. Ежегодно этот невидимый враг «съедает» около 13 млн. т металла.
Для сравнения – металлургическая промышленность стран Евросоюза в прошлом, 2014 году произвела всего на 0,5 млн. тонн больше. И это только – прямые потери.
А длительная эксплуатация стальных изделий без их эффективной защиты от коррозии вообще невозможна.
Что такое коррозия и её разновидности
Основной причиной интенсивного окисления поверхности металлов (что и является основной причиной коррозии) являются:
- Повышенная влажность окружающей среды.
- Наличие блуждающих токов.
- Неблагоприятный состав атмосферы.
Соответственно этому различают химическую, трибохимическую и электрохимическую природу коррозии. Именно они в совокупности своего влияния и разрушают основную массу металла.

Химическая коррозия
Такой вид коррозии обусловлен активным окислением поверхности металла во влажной среде. Безусловным лидером тут является сталь (исключая нержавеющую).
Железо, являясь основным компонентом стали, при взаимодействии с кислородом образует три вида окислов: FeO, Fe2O3 и Fe3O4.
Основная неприятность заключается в том, что определённому диапазону внешних температур соответствует свой окисел, поэтому практическая защита стали от коррозии наблюдается только при температурах выше 10000С, когда толстая плёнка высокотемпературного оксида FeO сама начинает предохранять металл от последующего образования ржавчины. Это процесс называется воронением, и активно применяется в технике для защиты поверхности стальных изделий. Но это – частный случай, и таким способом активно защищать металл от коррозии в большинстве случаев невозможно.
 Химическая коррозия активизируется при повышенных температурах. Склонность металлов к химическому окислению определяется значением их кислородного потенциала – способности к участию в окислительно-восстановительных реакциях. Сталь – ещё не самый худший вариант: интенсивнее её окисляются, в частности, свинец, кобальт, никель.
Химическая коррозия активизируется при повышенных температурах. Склонность металлов к химическому окислению определяется значением их кислородного потенциала – способности к участию в окислительно-восстановительных реакциях. Сталь – ещё не самый худший вариант: интенсивнее её окисляются, в частности, свинец, кобальт, никель.
Электрохимическая коррозия
Эта разновидность коррозии более коварна: разрушение металла в данном случае происходит при совокупном влиянии воды и почвы на стальную поверхность (например, подземных трубопроводов).
Влажный грунт, являясь слабощёлочной средой, способствует образованию и перемещению в почве блуждающих электрических токов. Они являются следствием ионизации частиц металла в кислородсодержащей среде, и инициирует перенос катионов металла с поверхности вовне.
Борьба с такой коррозией усложняется труднодоступностью диагностирования состояния грунта в месте прокладки стальной коммуникации.
Электрохимическая коррозия возникает при окислении контактных устройств линий электропередач при увеличении зазоров между элементами электрической цепи. Помимо их разрушения, в данном случае резко увеличивается энергопотребление устройств.

Трибохимическая коррозия
Данному виду подвержены металлообрабатывающие инструменты, которые работают в режимах повышенных температур и давлений. Антикоррозионное покрытие резцов, пуансонов, фильер и пр. невозможно, поскольку от детали требуется высокая поверхностная твёрдость.
Между тем, при скоростном резании, холодном прессовании и других энергоёмких процессах обработки металлов начинают происходить механохимические реакции, интенсивность которых возрастает с увеличением температуры на контактной поверхности «инструмент-заготовка».
Образующаяся при этом окись железа Fe2O3 отличается повышенной твёрдостью, и поэтому начинает интенсивно разрушать поверхность инструмента.

Методы борьбы с коррозией
Выбор подходящего способа защиты поверхности от образования ржавчины определяется условиями, в которых работает данная деталь или конструкция. Наиболее эффективны следующие методы:
- Нанесение поверхностных атмосферостойких покрытий;
- Поверхностная металлизация;
- Легирование металла элементами, обладающими большей стойкостью к участию в окислительно-восстановительных реакциях;
- Изменение химического состава окружающей среды.
Механические поверхностные покрытия
Поверхностная защита металла может быть выполнена его окрашиванием либо нанесением поверхностных плёнок, по своему составу нейтральных к воздействию кислорода. В быту, а также при обработке сравнительно больших площадей (главным образом, подземных трубопроводов) применяется окраска.
Среди наиболее стойких красок – эмали и краски, содержащие алюминий.
В первом случае эффект достигается перекрытием доступа кислороду к стальной поверхности, а во втором – нанесением алюминия на поверхность, который, являясь химически инертным металлом, предохраняет сталь от коррозионного разрушения.
Положительными особенностями данного способа защиты являются лёгкость его реализации и сравнительно небольшие финансовые затраты, поскольку процесс достаточно просто механизируется. Вместе с тем долговечность такого способа защиты невелика, поскольку, не обладая большой степенью сродства с основным металлом, такие покрытия через некоторое время начинают механически разрушаться.

Химические поверхностные покрытия
Коррозионная защита в данном случае происходит вследствие образования на поверхности обрабатываемого металла химической плёнки, состоящей из компонентов, стойких к воздействию кислорода, давлений, температур и влажности. Например, углеродистые стали обрабатывают фосфатированием.
Процесс может выполняться как в холодном, так и в горячем состоянии, и заключается в формировании на поверхности металла слоя из фосфатных солей марганца и цинка. Аналогом фосфатированию выступает оксалатирование – процесс обработки металла солями щавелевой кислоты.
Применением именно таких технологий повышают стойкость металлов от трибохимической коррозии.
Недостатком данных методов является трудоёмкость и сложность их применения, требующая наличия специального оборудования. Кроме того, конечная поверхность изменяет свой цвет, что не всегда приемлемо по эстетическим соображениям.
Легирование и металлизация
В отличие от предыдущих способов, здесь конечным результатом является образование слоя металла, химически инертного к воздействию кислорода. К числу таких металлов относятся те, которые на линии кислородной активности находятся возможно дальше от водорода. По мере возрастания эффективности этот ряд выглядит так: хром→медь→цинк→серебро→алюминий→платина.
Различие в технологиях получения таких антикоррозионных слоёв состоит в способе их нанесения.
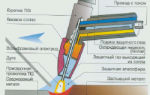
При металлизации на поверхность направляется ионизированный дуговой поток мелкодисперсного напыляемого металла, а легирование реализуется в процессе выплавки металла, как следствие протекания металлургических реакций между основным металлом и вводимыми легирующими добавками.

Изменение состава окружающей среды
В некоторых случаях существенного снижения коррозии удаётся добиться изменением состава атмосферы, в которой работает защищаемая металлоконструкция. Это может быть вакуумирование (для сравнительно небольших объектов), или работа в среде инертных газов (аргон, неон, ксенон).
Данный метод весьма эффективен, однако требует дополнительного оборудования – защитных камер, костюмов для обслуживающего персонала и т.д.
Используется он главным образом, в научно-исследовательских лабораториях и опытных производствах, где специально поддерживается необходимый микроклимат.
Кто нам мешает, тот нам поможет
В завершение укажем и на довольно необычный способ коррозионной защиты: с помощью самих окислов железа, точнее, одного из них – закиси-окиси Fe3O4. Данное вещество образуется при температурах 250…5000С и по своим механическим свойствам представляет собой высоковязкую технологическую смазку.
Присутствуя на поверхности заготовки, Fe3O4 перекрывает доступ кислороду воздуха при полугорячей деформации металлов и сплавов, и тем самым блокирует процесс зарождения трибохимической коррозии. Это явление используется при скоростной высадке труднодеформируемых металлов и сплавов.
Эффективность данного способа обусловлена тем, что при каждом технологическом цикле контактные поверхности обновляются, а потому стабильность процесса регулируется автоматически.
Оставляете заявку на сайте или по телефону
Оцениваем запрос и тех. документацию
Осматриваем объект
Подготавливаем КП
Сдаем работу заказчику
Выполняем работы
Разрабатываем рабочую документацию
Заключаем договор
Наши преимущества
Подготовленный персонал, находящийся постоянно в штате
Наличие богатого технического оснащения
Гарантийное и послегарантийное обслуживание
Самый большой спектр услуг в России
Большой опыт работы на разнотипных объектах
Коррозия металлов. Виды коррозии металлов
- Материалы из металлов под химическим или электрохимическим воздействием окружающей среды подвергаются разрушению, которое называется коррозией.
- Коррозия металлов вызывается окислительно-восстановительными реакциями, в результате которых металлы переходят в окисленную форму и теряют свои свойства, что приводит в негодность металлические материалы.
- Можно выделить 3 признака, характеризующих коррозию:
- Коррозия – это с химической точки зрения процесс окислительно-восстановительный.
- Коррозия – это самопроизвольный процесс, возникающий по причине неустойчивости термодинамической системы металл – компоненты окружающей среды.
- Коррозия – это процесс, который развивается в основном на поверхности металла. Однако, не исключено, что коррозия может проникнуть и вглубь металла.
Наиболее часто встречаются следующие виды коррозии металлов:
- Равномерная – охватывает всю поверхность равномерно
- Неравномерная
- Избирательная
- Местная пятнами – корродируют отдельные участки поверхности
- Язвенная (или питтинг)
- Точечная
- Межкристаллитная – распространяется вдоль границ кристалла металла
- Растрескивающая
- Подповерхностная
Основные виды коррозии металлов
С точки зрения механизма коррозионного процесса можно выделить два основных типа коррозии: химическую и электрохимическую.
Химическая коррозия металлов — это результат протекания таких химических реакций, в которых после разрушения металлической связи, атомы металла и атомы, входящие в состав окислителей, образуют химическую связь.
Электрический ток между отдельными участками поверхности металла в этом случае не возникает. Такой тип коррозии присущ средам, которые не способны проводить электрический ток – это газы, жидкие неэлектролиты.
Виды химической коррозии
Химическая коррозия металлов бывает газовой и жидкостной.
Газовая коррозия металлов – это результат действия агрессивных газовых или паровых сред на металл при высоких температурах, при отсутствии конденсации влаги на поверхности металла.
Это, например, кислород, диоксид серы, сероводород, пары воды, галогены.
Такая коррозия в одних случаях может привести к полному разрушению металла (если металл активный), а в других случаях на его поверхности может образоваться защитная пленка (например, алюминий, хром, цирконий).
Жидкостная коррозия металлов– может протекать в таких неэлектролитах, как нефть, смазочные масла, керосин и др. Этот тип коррозии при наличии даже небольшого количества влаги, может легко приобрести электрохимический характер.
При химической коррозии скорость разрушения металла пропорциональна скорости химической реакции и той скорости с которой окислитель проникает сквозь пленку оксида металла, покрывающую его поверхность. Оксидные пленки металлов могут проявлять или не проявлять защитные свойства, что определяется сплошностью.
Фактор Пиллинга-Бэдворса
- Сплошность такой пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе) по отношению объема образовавшегося оксида или другого какого-либо соединения к объему израсходованного на образование этого оксида металла
- α = Vок/VМе = Мок·ρМе/(n·AMe·ρок),
- где Vок — объем образовавшегося оксида
- VМе — объем металла, израсходованный на образование оксида
- Мок – молярная масса образовавшегося оксида
- ρМе – плотность металла
- n – число атомов металла
- AMe — атомная масса металла
- ρок — плотность образовавшегося оксида
Оксидные пленки, у которых α < 1, не являются сплошными и сквозь них кислород легко проникает к поверхности металла. Такие пленки не защищают металл от коррозии. Они образуются при окислении кислородом щелочных и щелочно-земельных металлов (исключая бериллий).
- Оксидные пленки, у которых 1 < α < 2,5 являются сплошными и способны защитить металл от коррозии.
- При значениях α > 2,5 условие сплошности уже не соблюдается, вследствие чего такие пленки не защищают металл от разрушения.
- Ниже представлены значения сплошности α для некоторых оксидов металлов
| Металл | Оксид | α | Металл | Оксид | α |
| K | K2O | 0,45 | Zn | ZnO | 1,55 |
| Na | Na2O | 0,55 | Ag | Ag2O | 1,58 |
| Li | Li2O | 0,59 | Zr | ZrO2 | 1.60 |
| Ca | CaO | 0,63 | Ni | NiO | 1,65 |
| Sr | SrO | 0,66 | Be | BeO | 1,67 |
| Ba | BaO | 0,73 | Cu | Cu2O | 1,67 |
| Mg | MgO | 0,79 | Cu | CuO | 1,74 |
| Pb | PbO | 1,15 | Ti | Ti2O3 | 1,76 |
| Cd | CdO | 1,21 | Cr | Cr2O3 | 2,07 |
| Al | Al2O2 | 1,28 | Fe | Fe2O3 | 2,14 |
| Sn | SnO2 | 1,33 | W | WO3 | 3,35 |
| Ni | NiO | 1,52 |
Электрохимическая коррозия металлов – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
При таком типе коррозии атом удаляется из кристаллической решетки результате двух сопряженных процессов:
- Анодного – металл в виде ионов переходит в раствор.
- Катодного – образовавшиеся при анодном процессе электроны, связываются деполяризатором (вещество — окислитель).
- Сам процесс отвода электронов с катодных участков называется деполяризацией, а вещества способствующие отводу – деполяризаторами.
- Наибольшее распространение имеет коррозия металлов с водородной и кислородной деполяризацией.
- Водородная деполяризация
- Водородная деполяризация осуществляется на катоде при электрохимической коррозии в кислой среде:
- 2H++2e— = H2 разряд водородных ионов
- 2H3O++2e— = H2 + 2H2O
- Кислородная деполяризация
- Кислородная деполяризация осуществляется на катоде при электрохимической коррозии в нейтральной среде:
- O2 + 4H++4e— = H2O восстановление растворенного кислорода
- O2 + 2H2O + 4e— = 4OH—
- Все металлы, по их отношению к электрохимической коррозии, можно разбить на 4 группы, которые определяются величинами их стандартных электродных потенциалов:
- Активные металлы (высокая термодинамическая нестабильность) – это все металлы, находящиеся в интервале щелочные металлы — кадмий (Е0 = -0,4 В). Их коррозия возможна даже в нейтральных водных средах, в которых отсутствуют кислород или другие окислители.
- Металлы средней активности (термодинамическая нестабильность) – располагаются между кадмием и водородом (Е0 = 0,0 В). В нейтральных средах, в отсутствии кислорода, не корродируют, но подвергаются коррозии в кислых средах.
- Малоактивные металлы (промежуточная термодинамическая стабильность) – находятся между водородом и родием (Е0 = +0,8 В). Они устойчивы к коррозии в нейтральных и кислых средах, в которых отсутствует кислород или другие окислители.
- Благородные металлы (высокая термодинамическая стабильность) – золото, платина, иридий, палладий. Могут подвергаться коррозии лишь в кислых средах при наличии в них сильных окислителей.
Виды электрохимической коррозии
Электрохимическая коррозия может протекать в различных средах. В зависимости от характера среды выделяют следующие виды электрохимической коррозии:
- Коррозия в растворах электролитов — в растворах кислот, оснований, солей, в природной воде.
- Атмосферная коррозия – в атмосферных условиях и в среде любого влажного газа. Это самый распространенный вид коррозии.
- Например, при взаимодействии железа с компонентами окружающей среды, некоторые его участки служат анодом, где происходит окисление железа, а другие – катодом, где происходит восстановление кислорода:
- А: Fe – 2e— = Fe2+
- K: O2 + 4H+ + 4e— = 2H2O
- Катодом является та поверхность, где больше приток кислорода.
- Почвенная коррозия – в зависимости от состава почв, а также ее аэрации, коррозия может протекать более или менее интенсивно. Кислые почвы наиболее агрессивны, а песчаные – наименее.
- Аэрационная коррозия — возникает при неравномерном доступе воздуха к различным частям материала.
- Морская коррозия – протекает в морской воде, в связи с наличием в ней растворенных солей, газов и органических веществ.
- Биокоррозия – возникает в результате жизнедеятельности бактерий и других организмов, вырабатывающих такие газы как CO2, H2S и др., способствующие коррозии металла.
- Электрокоррозия – происходит под действием блуждающих токов на подземных сооружениях, в результате работ электрических железных дорог, трамвайных линий и других агрегатов.
Основной способ защиты от коррозии металла – это создание защитных покрытий – металлических, неметаллических или химических.
Металлическое покрытие наносится на металл, который нужно защитить от коррозии, слоем другого металла, устойчивого к коррозии в тех же условиях.
Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный) , чем защищаемый, то оно называется анодным покрытием.
Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием.
Например, при нанесении слоя цинка на железо, при нарушении целостности покрытия, цинк выступает в качестве анода и будет разрушаться, а железо защищено до тех пор, пока не израсходуется весь цинк. Цинковое покрытие является в данном случае анодным.
Катодным покрытием для защиты железа, может, например, быть медь или никель. При нарушении целостности такого покрытия, разрушается защищаемый металл.
Такие покрытия могут быть неорганические (цементный раствор, стекловидная масса) и органические (высокомолекулярные соединения, лаки, краски, битум).
Химические покрытия
- В этом случае защищаемый металл подвергают химической обработке с целью образования на поверхности пленки его соединения, устойчивой к коррозии. Сюда относятся:
- оксидирование – получение устойчивых оксидных пленок (Al2O3, ZnO и др.
);
- фосфатирование – получение защитной пленки фосфатов (Fe3(PO4)2, Mn3(PO4)2);
- азотирование – поверхность металла (стали) насыщают азотом;
- воронение стали – поверхность металла взаимодействует с органическими веществами;
- цементация – получение на поверхности металла его соединения с углеродом.
Изменение состава технического металла также способствует повышению стойкости металла к коррозии. В этом случае в металл вводят такие соединения, которые увеличивают его коррозионную стойкость.
Изменение состава коррозионной среды (введение ингибиторов коррозии или удаление примесей из окружающей среды) тоже является средством защиты металла от коррозии.
Электрохимическая защита
Электрохимическая защита основывается на присоединении защищаемого сооружения катоду внешнего источника постоянного тока, в результате чего оно становится катодом. Анодом служит металлический лом, который разрушаясь, защищает сооружение от коррозии.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Примеры задач с решениями на определение защитных свойств оксидных пленок, определение коррозионной стойкости металлов, а также уравнения реакций, протекающих при электрохимической коррозии металлов приведены в разделе Задачи к разделу Коррозия металлов
Коррозия металлов и способы защиты от нее
| Коррозия – это процесс разрушения металлов и металлических конструкций под воздействием различных факторов окружающей среды – кислорода, влаги, вредных примесей в воздухе. |
Коррозионная стойкость металла зависит от его природы, характера среды и температуры.
- Благородные металлы не подвергаются коррозии из-за химической инертности.
- Металлы Al, Ti, Zn, Cr, Ni имеют плотные газонепроницаемые оксидные плёнки, которые препятствуют коррозии.
- Металлы с рыхлой оксидной плёнкой – Fe, Cu и другие – коррозионно неустойчивы. Особенно сильно ржавеет железо.
Различают химическую и электрохимическую коррозию.
| Химическая коррозия сопровождается химическими реакциями. Как правило, химическая коррозия металлов происходит при действии на металл сухих газов, её также называют газовой. |
- 3Fe + 2O2 = Fe3O4
- При химической коррозии также возможны процессы:
- Fe + 2HCl → FeCl2 + H2
- 2Fe + 3Cl2 → 2FeCl3
- Как правило, такие процессы протекают в аппаратах химических производств.
| Электрохимическая коррозия – это процесс разрушения металла, который сопровождается электрохимическими процессами. Как правило, электрохимическая коррозия протекает в присутствии воды и кислорода, либо в растворах электролитов. |
В таких растворах на поверхности металла возникают процессы переноса электронов от металла к окислителю, которым является либо кислород, либо кислота, содержащаяся в растворе.
При этом электродами являются сам металл (например, железо) и содержащиеся в нем примеси (обычно менее активные металлы, например, олово).
В таком загрязнённом металле идёт перенос электронов от железа к олову, при этом железо (анод) растворяется, т.е. подвергается коррозии:
- Fe –2e = Fe 2+
- На поверхности олова (катод) идёт процесс восстановления водорода из воды или растворённого кислорода:
- 2H+ + 2e → H2
- O2 + 2H2O + 4e → 4OH–
| Например, при контакте железа с оловом в растворе соляной кислоты происходят процессы: |
- Анод: Fe –2e → Fe 2+
- Катод: 2H+ + 2e → H2
- Суммарная реакция: Fe + 2H+ → H2 + Fe2+
- Если реакция проходит в атмосферных условиях в воде, в ней участвует кислород и происходят процессы:
- Анод: Fe –2e → Fe 2+
- Катод: O2 + 2H2O + 4e → 4OH–
- Суммарная реакция:
- Fe 2+ + 2OH – → Fe(OH)2
- 4Fe(OH)2 + O2+ 2H2O → 4Fe(OH)3
- При этом образуется ржавчина.
Защитные покрытия
Защитные покрытия предотвращают контакт поверхности металла с окислителями.
- Катодное покрытие – покрытие менее активным металлом (защищает металл только неповреждённое покрытие).
- Покрытие краской, лаками, смазками.
- Создание на поверхности некоторых металлов прочной оксидной плёнки химическим путём (анодирование алюминия, кипячение железа в фосфорной кислоте).
Создание сплавов, стойких к коррозии
Физические свойства сплавов могут существенно отличаться от свойств чистых металлов. Добавление некоторых металлов может приводить к повышению коррозионной стойкости сплава. Например, нержавеющая сталь, новые сплавы с большой коррозионной устойчивостью.
Изменение состава среды
Коррозия замедляется при добавлении в среду, окружающую металлическую конструкцию, ингибиторов коррозии. Ингибиторы коррозии — это вещества, подавляющие процессы коррозии.
Электрохимические методы защиты
Протекторная защита: при присоединении к металлической конструкции пластинок из более активного металла – протектора. В результате идёт разрушение протектора, а металлическая конструкция при этом не разрушается.
Способы борьбы с коррозией металлов
Коррозией металла называется нарушение его структуры в результате химических или электрохимических реакций. Это может приводить к разрушению деталей, конструкций, приводить к выходу из строя узлов автомобилей, станков, другого производственного оборудования, инструментов, трубопроводов и иных металлических изделий. Каждый год коррозия разрушает около 13 миллионов тонн металла.
Предотвратить и замедлить этот негативный процесс призваны меры антикоррозийной защиты металла. На это в мире тратится ежегодно более 2,5 триллионов долларов США, по данным NACE International. Как показывает практика, металлические изделия просто не способны служить без специальных защитных мер в течение длительного времени
Причины коррозии металлов
Основными «виновниками» коррозии являются воздействие природных факторов – воды и повышенной влажности, высокой температуры, кислых веществ с содержанием сульфатов и хлоридов, взвешенных в воздухе частиц различных веществ, солей, промышленных смазочных составов.
Виды коррозии металлов
В зависимости от того, какие именно реакции протекают на границе металла с окружающей средой, выделяют три основных вида коррозии.
- Химическая развивается, когда металл соприкасается с солями или сухими газообразными соединениями. Яркий пример – контакт днища кузова автомобиля с солью, которой зимой в России посыпают автодороги. На деталях машин образуется слой из солей натрия и калия, разъедающих сталь и любой другой металл.
- Электрохимическая происходит при соприкосновении с водой. Встречается чаще других видов.
- Биологическая (биокоррозия) заключается в том, что поверхность металла разрушают микроорганизмы или радиоактивное излучение.
В соответствии с формой поражения коррозия может быть точечной, когда появляются узкие глубокие отверстия внутри металла с сохранением целостности поверхности. Она чаще наблюдается в изделиях из алюминиевых сплавов и нержавеющей стали.
Второй тип – равномерная коррозия, проявляющаяся на поверхности металла в виде равномерного слоя отложений. Третий – щелевая, захватывает участки с небольшими углублениями, где накапливается влага.
Четвертый – межкристаллическая, развивается в зернистой структуре металла, приводя к локальным повреждениям.
Выделяют также коррозионное растрескивание, когда под действием агрессивной среды в сочетании с постоянной или периодической высокой нагрузкой в металле появляются трещины.
Способы борьбы с коррозией
Сегодня применяются различные способы защиты металлов от коррозии. Выбор определяется условиями эксплуатации металлических изделий, в том числе климатом региона, характеристиками самой металлической конструкции, а также совместимостью антикоррозийного состава и обрабатываемого материала, другими факторами.
Все виды борьбы с коррозией металла можно разделить на три основных, направленных на изменение одного из факторов:
- свойств самого металла;
- свойств окружающей среды;
- характера взаимодействия металлического изделия и среды на границе контакта.
Изменение свойств металла для предотвращения коррозии
В эту группу методов включаются легирование, поверхностная и термическая обработка. Первые два можно отнести к химическим методам. Третий – к технологическим методам.
Легирование предполагает включение в состав металла в процессе его производства химических элементов, которые наименее склонны вступать в химическую реакцию с кислородом. Эти компоненты по возрастанию химической эффективности располагаются в следующем порядке: хром, медь, цинк, серебро, алюминий, платина.
Другой способ – металлизация (гальванический метод), когда поверхность изделия покрывается более устойчивым к действию кислорода металлом. Он подается в мелкодисперсном виде в форме ионизированного потока. Сюда относятся холодное цинкование и горячее цинкование.
Для защиты от коррозии могут также применяться фосфатирование или оксалатирование – обработка поверхности металла фосфатными солями марганца и цинка, либо щавелевой кислоты.
Термическая обработка означает нагрев металла до температуры выше +900◦С. Как правило, применяется в сочетании с насыщением поверхности заготовки хромом, азотом, алюминием, кремнием и другими элементами, повышающими сопротивляемость металла коррозии.
Перечисленные выше методы защиты относят к активным. Сюда же можно причислить и преобразование структуры двойного электрического слоя – анодирование.
На металлическую поверхность воздействуют постоянным электрическим полем с заданными параметрами напряжения, которые подбираются в соответствии со свойствами металла.
Это увеличивает его электродный потенциал и повышает устойчивость к коррозии верхнего слоя. Такой способ обычно используют для создания антикоррозийной защиты алюминия.
Изменение свойств окружающей среды
Параметры окружающей металлическое изделие среды можно менять с помощью ее ингибирования, обескислороживания, осушения воздушной смеси и устранения агрессивных веществ – солей, кислот и других.
Если объект небольшой, вокруг него может создаваться вакуум: в воздухе практически не остается кислорода, соответственно, риск появления коррозии минимизируется.
Другой метод – заполнение пространства вокруг металлической детали или конструкции инертным газом (неоном, ксеноном, аргоном).
Этот способ дает высокий эффект, но довольно сложен в применении: необходимо обустройство защитной камеры, а также наличие специальных защитных костюмов для людей, обслуживающих оборудование из металла.
Его используют обычно в научно-исследовательских лабораториях и на опытных производственных участках, где требуется поддерживать особый микроклимат.
Изменение характера взаимодействия металла со средой
Это антикоррозийная обработка металла, для которой применяется большое разнообразие способов.
- Защитные покрытия – лаков и красок, масел, смазок и так далее.
- Устранение катодной поляризации в форме защиты от коррозии контактного типа, электродренажа, удаления блуждающих токов и так далее.
- Грамотное проектирование металлических конструкций, при котором подбирается наиболее устойчивый к действию факторов конкретной среды металл, устраняются зазоры, застойные зоны, соприкосновения разнородных металлов, и так далее.
Для борьбы с коррозией металлов широко распространены лакокрасочные покрытия. На сегодняшний день этот вариант применяется особенно часто.
Используются специальные органические ЛКМ, компоненты которых не вступают в реакцию с кислородом, в также составы с алюминием. Первые перекрывают доступ О₂.
Вторые не допускают коррозионного разрушения стали за счет наличия в составе химически инертного элемента – алюминия. Кроме того, используют защитные пленки и жидкий пластик – относительно новое решение.
На эффективность такой защиты влияют качество подготовки металлической поверхности к нанесению покрытия, равномерность его нанесения, толщина и прочность слоя, исключение образования воздушных полостей и другие факторы.
Этот способ отличается простотой реализации и низкими финансовыми затратами. Однако эффект недолговечен: со временем происходит механическое разрушение покрытия.
Важно также понимать, что ЛКМ и пленки препятствуют появлению коррозии, но не способны его предотвратить, что дает основания называть данный способом защиты от коррозии пассивным.
Можно покрыть ржавый металл специальной краской, которая трансформирует ржавчину и создаст антикоррозийный защитный слой.
К необычным способам относится высоковязкая технологическая смазка из окислов железа – закиси-окиси Fe3O4. Температура образования данного вещества составляет +250-500◦С. Им можно обработать металл, чтобы не ржавел.
Образуя на поверхности плотную пленку, Fe3O4 не дает кислороду проникать к металлу, не позволяя развиваться трибохимической коррозии.
Данный метод применяется на металлургических предприятиях в процессе скоростной высадки сплавов и металлов труднодеформируемых типов.
Способы удаления коррозии
Если ржавчина на металле уже появилась, риск разрушения деталей или конструкций резко возрастает. Необходимо удалить коррозию, для чего предлагается использовать один из способов.
- Ручная механическая очистка – традиционный вариант. Поверхность изделия обрабатывается металлической щеткой, наждачной бумагой либо абразивным кругом. Можно делать это вручную или с помощью дрели с соответствующей насадкой, либо углошлифовальной машины. Метод требует больших усилий и много времени.
- Специальные химические составы, вступающие в реакцию с оксидом железа. Данный вариант актуален для изделий, форма которых сложная, поверхность рифленая. Однако применять этот метод на изделиях с неметаллическими компонентами нельзя. Кроме того, работа с такими средствами требует особой осторожности, поскольку они могут нанести вред здоровью человека.
- Электрохимический способ. Металлическое изделие опускают в раствор электролита, подключив к источнику электротоку. Ток, проходящий через электролит и деталь, заставляет слой ржавчины отделяться от ее поверхности. Но этот вариант подходит не для всех изделий из металла.
- Пескоструйная и дробеструйная обработка, ультразвук очищают металл от оксида железа, отбивая его от поверхности.
- Сухой лед (криобластинг) – очищение с помощью струи из гранул сухого льда. При ударе о металл происходит испарение частичек льда. Высвобождается углекислый газ: мгновенно расширяясь, он захватывает и удаляет ржавчину.
Вложения в защиту металла от коррозии позволяют продлить срок службы деталей и конструкций, а, значит, увеличить периодичность их замены.
Максимальный эффект дает сочетание нескольких методов. Например, для сохранения металлических элементов, находящихся под водой, применяют комбинацию катодной защиты и ЛКМ. Антикоррозийная защита направляющих насадок гребных винтов включает применение коррозионностойкой стали, электроразъединение разнородных материалов, катодную защиту и ЛКМ.
Коррозия металла – причины появления и способы защиты
Все без исключения металлы, используемые для изготовления различных механизмов и конструкций, подвержены разрушению вследствие взаимодействия с внешней средой. Это процесс известен как коррозия. Для увеличения срока службы данных материалов используются различные способы, узнать о которых можно в интернет-журнале gidpokraske.
Причины возникновения коррозии
Разрушение металлов под воздействием коррозионных процессов вызывается многими причинами. Наибольший вред наносят химические и электрохимические коррозионные процессы.
В первом случае в ходе химических реакций образуются соединения металлов с различными агрессивными веществами, присутствующими в окружающей среде.
Во втором случае металлы растворяются в электролитах, которые образуются в воздухе или воде.
Кроме того, металлы страдают от коррозии вследствие воздействия радиации и различных микроорганизмов. Механические напряжения ускоряют коррозионные процессы, так как они уменьшают термостойкость металлов, повреждают присутствующие на их поверхности оксидные пленки и способствуют возникновению трещин и неоднородностей.
Существуют следующие виды коррозии:
- местная (затрагивает только отдельные участки поверхности металлов);
- равномерная (охватывает всю поверхность металлов);
- межкристаллитная (проявляется в разрушении металлов по границам зерен).
Способы защиты металлов от химической коррозии
Полностью предотвратить разрушение металлов в результате химического взаимодействия с агрессивными веществами, присутствующими в окружающей среде, невозможно. Однако этот процесс можно значительно замедлить. Для решения данной задачи используются следующие способы:
- уменьшение агрессии окружающей среды;
- повышение коррозиеустойчивости металла;
- исключение контакта между металлом и агрессивными веществами из окружающей среды.
Чтобы повысить коррозиеустойчивость стали, в нее включают легирующие добавки. Для покрытия металлов в целях противокоррозийной защиты используются другие металлы или неметаллические составы. Например, железо защищается от коррозии путем нанесения на его поверхность алюминия, цинка или никеля. Покрытия из
ТОП-10 — Список лучших игр-стратегий на компьютер
неметаллических составов выполняются при помощи разнообразных красок, лаков и полимеров, которые формируют на поверхности металлов защитную пленку, предотвращающую их контакт с окружающей средой.
Преимущество использования красок и лаков заключается в наличии возможности наносить их на месте установки металлических конструкций.
Кроме того, этот способ не требует больших затрат времени и денег и может применяться неоднократно по мере необходимости.
Способы защиты металлов от электрохимической коррозии
Чтобы уменьшить интенсивность разрушения металлов под воздействием электрохимической коррозии, нужно снизить коррозионную активность окружающей среды путем введения в нее неметаллических ингибиторов и сократить объем веществ, способных вступить в электрохимическую реакцию. В этих целях снижают кислотность грунтов и водных растворов, которые контактируют с металлическими изделиями. Для уменьшения электрохимической коррозии заглубленных металлических конструкций и подземных коммуникаций используются следующие способы:
- участки металлоконструкций, служащие источником блуждающего электротока, соединяют металлическим проводом с рельсом трамвайных путей;
- теплотрассы располагают как можно дальше от рельсов, по которым движется электрический транспорт;
- переходное сопротивление между почвой и трубопроводами повышают при помощи электроизоляционных трубных опор.
Загрузка…